
Investigación sobre el dolor de cabeza
La investigación es clave para seguir avanzando en el diagnóstico y el tratamiento del dolor de cabeza. ¿Eres paciente y quieres contribuir?
Tu participación en ensayos clínicos puede ser de gran ayuda.
Introducción
o reducir la intensidad el dolor, sin embargo, no existen terapias que lo eliminen definitivamente.
Además, en muchos casos, los fármacos son poco efectivos, y su efecto es variable en el tiempo y según el paciente. Por ello, la investigación
es continua y fundamental para que los pacientes podamos conseguir un mejor diagnóstico y tratamiento de nuestra enfermedad.
Actualmente, algunos de los principales campos de investigación se centran, por ejemplo, en detectar nuevas tipologías de dolor de cabeza
no clasificadas, en estudios epidemiológicos para obtener información más precisa de la incidencia de las distintas cefaleas, en estudios genéticos
para analizar e identificar los genes responsables del dolor provocado por esta enfermedad y en la investigación con técnicas de neuroimagen
para conocer mejor los procesos neuronales y su relación con la aparición del dolor.
¿Eres paciente y quieres implicarte en la investigación? Descubre los ensayos clínicos
¿Qué son?
Estudios de investigación que prueban un nuevo fármaco en un grupo de personas
afectadas por una enfermedad determinada.
También se utilizan cuando un tratamiento ya está disponible. En este caso, permiten identificar su potencial para tratar
nuevas patologías, recoger información sobre su eficacia y seguridad a largo plazo, examinar cómo está siendo prescrito por médicos
y usado por pacientes fuera de ensayos clínicos y para poder mejorar su formulación.
¿Por qué participar?
¿Cuál es su objetivo?
Analizan…
- La eficacia del medicamento, es decir, que tenga efectos positivos en la enfermedad y sus síntomas.
- La seguridad, comprobando si tiene efectos secundarios.
Para que las autoridades sanitarias aprueben el fármaco es obligatorio aprobar estos dos aspectos.
Las 4 fases del ensayo clínico
todo el proceso y las fases a superar para que se confirmen su eficacia y seguridad.
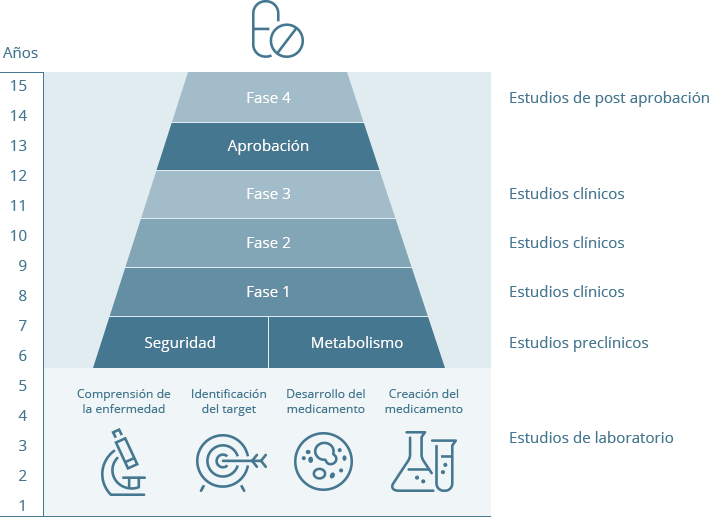
Fase 1
Se prueba el medicamento en voluntarios sanos para entender cómo interacciona con el cuerpo, y obtener información sobre cómo se tolera y qué efectos secundarios puede provocar.
Fase 2
Se prueba el medicamento en un grupo reducido de pacientes para examinar su eficacia y tolerabilidad. Aquí el objetivo es encontrar la dosis con mejor equilibrio tolerancia-efectos secundarios.
Fase 3
En esta fase suelen participar miles de pacientes. Permite a los investigadores comprobar que los resultados de la fase 2 son válidos incluso en un amplio número de pacientes y obtener más detalles sobre efectos secundarios, a menudo durante un periodo de tiempo más largo.
Aprobación
Antes de que pueda estar disponible en el mercado, el medicamento debe ser aprobado por las autoridades reguladoras de la zona donde se comercializará. En el caso de España, por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ( https://www.aemps.gob.es/home.htm), quien comprueba, en base a la información obtenida en los ensayos realizados, que el tratamiento ofrezca más beneficios que riesgos.
Fase 4
Tiene lugar una vez que el medicamento ya está a la venta y es útil para examinar cómo funciona en “situaciones reales”.
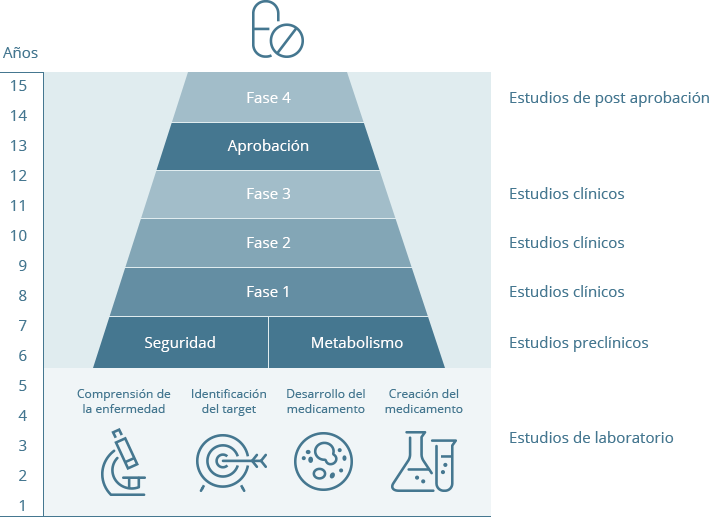
Fase 1
Se prueba el medicamento en voluntarios sanos para entender cómo interacciona con el cuerpo, y obtener información sobre cómo se tolera y qué efectos secundarios puede provocar.
Fase 2
Se prueba el medicamento en un grupo reducido de pacientes para examinar su eficacia y tolerabilidad. Aquí el objetivo es encontrar la dosis con mejor equilibrio tolerancia-efectos secundarios.
Fase 3
En esta fase suelen participar miles de pacientes. Permite a los investigadores comprobar que los resultados de la fase 2 son válidos incluso en un amplio número de pacientes y obtener más detalles sobre efectos secundarios, a menudo durante un periodo de tiempo más largo.
Aprobación
Antes de que pueda estar disponible en el mercado, el medicamento debe ser aprobado por las autoridades reguladoras de la zona donde se comercializará. En el caso de España, por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) ( https://www.aemps.gob.es/home.htm), quien comprueba, en base a la información obtenida en los ensayos realizados, que el tratamiento ofrezca más beneficios que riesgos.
Fase 4
Tiene lugar una vez que el medicamento ya está a la venta y es útil para examinar cómo funciona en “situaciones reales”.
Recuerda
- Para poder participar en un ensayo clínico debes cumplir con los criterios de inclusión que defina ese estudio. Son una serie de requisitos
que aseguran que los participantes son los adecuados, a quien se dirige el medicamento. - Antes de unirte a un ensayo clínico, tu médico te informará detalladamente sobre las ventajas y posibles riesgos.
- Puedes retirarte de un ensayo clínico en cualquier momento, sin tener que dar ninguna explicación.
¿Quieres participar?
Si te interesa participar en ensayos clínicos con medicamentos que se están desarrollando,
te explicamos cómo puedes hacerlo:
- Habla con tu médico. Él puede informarte sobre los ensayos clínicos que se están realizando e indicarte si cumples con el perfil para participar.
- También puedes consultar los ensayos clínicos que se están llevando a cabo en tu localidad en el Registro Español de Estudios Clínicos.
¿Necesitas más información?
Consulta cualquier duda con tu médico y recuerda que puedes formarte en temas de investigación y participación en ensayos clínicos
a través de la Academia Europea de Pacientes (EUPATI).
